Аминокислоты — это структурные звенья в цепочке белка, каждая из которых записана в ДНК специальным кодоном, или сочетанием трех «букв» последовательности (нуклеотидов). Большинство из них может быть закодировано несколькими способами, что повышает устойчивость системы копирования против мутаций. Однако такие синонимичные кодоны еще и управляют синтезом белка. Российские ученые предложили новый метод оценки влияния синонимичных замен кодонов в генах на производство клетками белка. Свои результаты ученые из ФИЦ Биотехнологии РАН опубликовали в International Journal of Molecular Sciences. Работа выполнена в рамках Федеральной научно-технич еской программы развития генетических технологий под эгидой нацпроекта «Наука и университеты».
 От построения мышц до регулирования различных химических реакций, от переноса кислорода в крови до расщепления питательных веществ — эти и многие другие функции выполняют белки. Состав всех белков организма кодируется в его геноме при помощи специального шифра: каждая аминокислота записана тремя нуклеотидами (кодон). Но большинство аминокислот могут быть закодированы несколькими разными синонимичными кодонами. Эта особенность генома помогает снизить влияние «однобуквенных» мутаций, ведь при синтезе аминокислота остается той же, и структура белка не «ломается». Со временем было выяснено, что разные синонимичные кодоны имеют и другие функции: например, защищать белок от преждевременной деградации или обеспечивать сворачивание в правильную структуру. Исследователи ФИЦ Биотехнологии РАН изучили синонимичные мутации E.coli (кишечной палочки) и придумали, как можно оценить масштабы их влияния на производство белков.
От построения мышц до регулирования различных химических реакций, от переноса кислорода в крови до расщепления питательных веществ — эти и многие другие функции выполняют белки. Состав всех белков организма кодируется в его геноме при помощи специального шифра: каждая аминокислота записана тремя нуклеотидами (кодон). Но большинство аминокислот могут быть закодированы несколькими разными синонимичными кодонами. Эта особенность генома помогает снизить влияние «однобуквенных» мутаций, ведь при синтезе аминокислота остается той же, и структура белка не «ломается». Со временем было выяснено, что разные синонимичные кодоны имеют и другие функции: например, защищать белок от преждевременной деградации или обеспечивать сворачивание в правильную структуру. Исследователи ФИЦ Биотехнологии РАН изучили синонимичные мутации E.coli (кишечной палочки) и придумали, как можно оценить масштабы их влияния на производство белков.
«Мы показали, что синонимичные замены кодонов — это основной фактор, влияющий на экспрессию генов — то есть, на количество синтезируемого белка. Так, при помощи синонимичных мутаций в гене gfp производство зеленого флуоресцентного белка может быть повышено в 250 раз! Благодаря развитию биотехнологий у нас есть базы с результатами анализа протеомов различных организмов. Это позволяет разрабатывать новые методы, лучше предсказывающие экспрессию, чтобы оптимизировать этот процесс, когда нам это необходимо», — рассказал ведущий автор работы Константин Зайцев, сотрудник ФИЦ Биотехнологии РАН.
Самые популярные способы предсказания экспрессии белков — это Codon Adaptation Index (CAI) и tRNA adaptation index (TAI). Однако в них используется множество упрощений, отрицательно влияющих на точность предсказания экспрессии. И поэтому коэффициент корреляции между предсказанными и реальными значениями для генов E.coli составляет 0,53-0,54, что не позволяет определить влияние синонимичных мутаций на этот параметр. Поэтому российские биотехнологи пошли другим путем: они показали, что средняя частота каждого кодона отличается между генами с разными уровнями экспрессии. После чего, проанализировали корреляции между частотами кодонов в генах и уровнями экспрессии соответствующих этим генам белков, и показали, что частота каждого кодона влияет на экспрессию индивидуально.
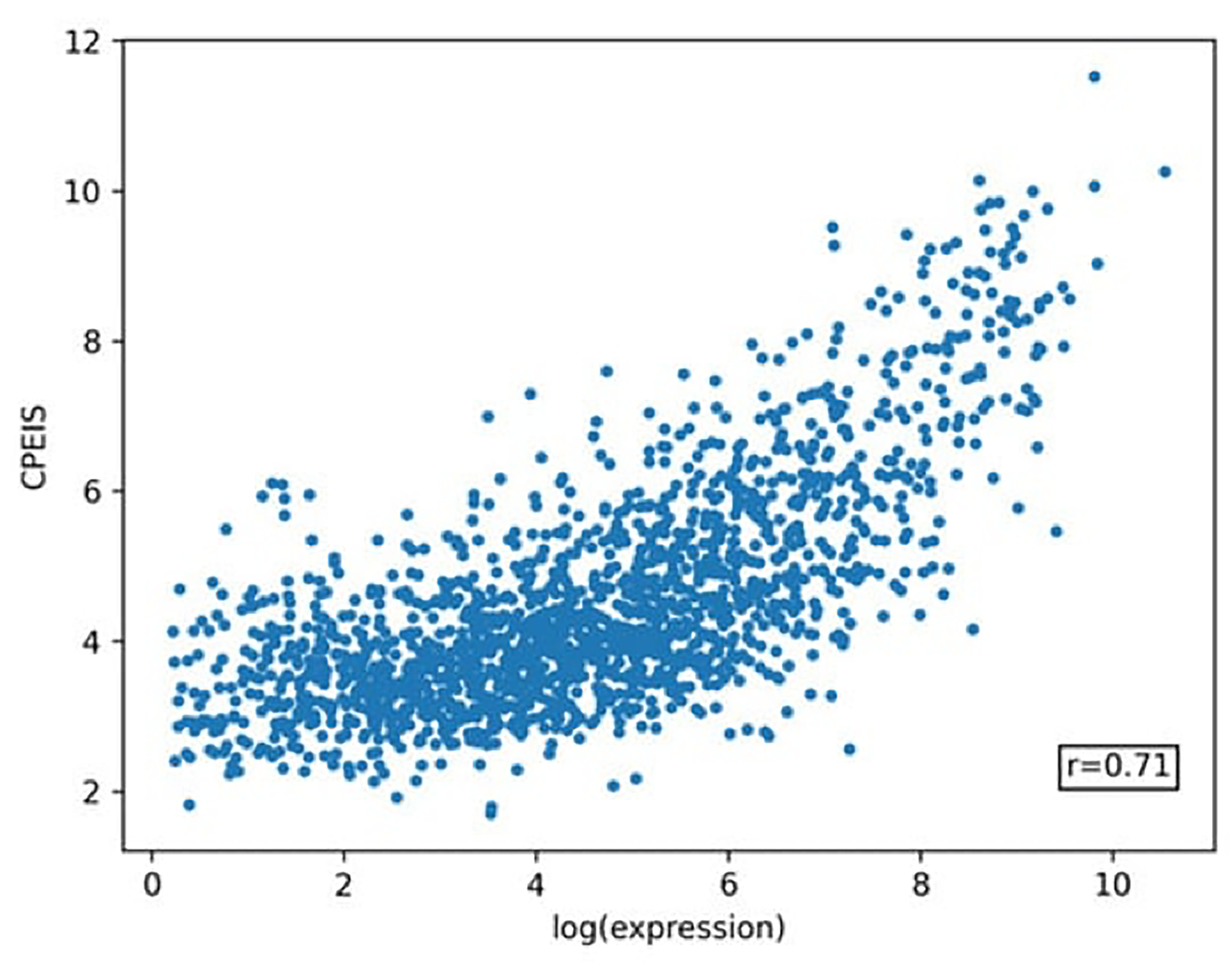 Ученые создали два индекса для оценки этой зависимости. Первый: статистический Codon Expression Index (CEI), показывает, как наличие кодона влияет на синтез нужного белка. Второй: эмпирический показатель Codon Productivity (CP), определяет, как конкретный вариант трехбуквенного «шифра» соотносится с суммарным количеством аминокислот, использованным в клетке для производства белка. Результаты обеих моделей хорошо согласуются между собой — их коэффициент корреляции составил 0,945. Затем биотехнологи сравнили экспериментальные данные по количеству белка в E.coli с этими моделями. Коэффициент корреляции индексов с реальными данными достиг 0,7, что значительно выше, чем у существующих аналогов.
Ученые создали два индекса для оценки этой зависимости. Первый: статистический Codon Expression Index (CEI), показывает, как наличие кодона влияет на синтез нужного белка. Второй: эмпирический показатель Codon Productivity (CP), определяет, как конкретный вариант трехбуквенного «шифра» соотносится с суммарным количеством аминокислот, использованным в клетке для производства белка. Результаты обеих моделей хорошо согласуются между собой — их коэффициент корреляции составил 0,945. Затем биотехнологи сравнили экспериментальные данные по количеству белка в E.coli с этими моделями. Коэффициент корреляции индексов с реальными данными достиг 0,7, что значительно выше, чем у существующих аналогов.
«Наши два новых индекса, которые определяют влияние частоты конкретного кодона на уровень экспрессии белка, по точности превосходят все традиционные методы. Они показывают, что частоты различных кодонов позволяют предсказать количество белка, которое производится на основании этогогена. Кроме того, мы выяснили, что самые распространенные версии кодонов не всегда самые эффективные», — прокомментировал автор работы Алексей Федоров, директор ФИЦ Биотехнологии РАН.